A Síndrome dos ovários policísticos foi inicialmente descrita por Stein e Leventhal em 1935, associando pela primeira vez o achado de ovários policísticos, já descritos na literatura médica pelo menos 100 anos antes, com alguns sinais e sintomas, como amenorreia, infertilidade, hirsutismo e obesidade. Esta síndrome se caracteriza por um quadro de anovulação crônica e hiperandrogenismo, normalmente acompanhado por ovários de aspecto multifoliculares.
Acredita-se que sua prevalência está em torno de 6% a 12% das mulheres em idade reprodutiva (dependendo do critério diagnóstico adotado), sendo considerada a mais comum anormalidade endócrina das mulheres nesta fase da vida. Sua alta prevalência já seria suficiente para mostrar a magnitude do problema, mas soma-se a isso alguns aspectos ligados aos danos estéticos causados pelo hiperandrogenismo e a associação com infertilidade, que resultam, muitas vezes, em distúrbios psicossociais e consequente comprometimento importante da qualidade de vida. Além disso, há associação direta entre SOP e doenças malignas (câncer de endométrio), doenças cardiovasculares (hipertensão e doenças isquêmicas cardíacas) e diabetes mellitus.
Na reprodução assistida, este grupo de pacientes merece tratamento individualizado. Por um lado, apresentam em geral bons resultados em ciclos de fertilização in vitro (FIV), com maior número de folículos, óvulos coletados e embriões formados que pacientes sem SOP. Entretanto, apresentam um risco aumentado de complicações relacionadas à Síndrome da Hiperestimulação Ovariana (SHO), portanto, sendo necessária muita atenção na escolha do protocolo, dose de gonadotrofina e no manejo da estimulação ovariana.
Frente a tudo isso, considera-se o estudo da SOP um dos tópicos mais importantes da endocrinologia reprodutiva feminina. Entretanto, apesar de muito investigada, sua definição ainda é controversa e há muitos aspectos fisiopatológicos ainda desconhecidos.
FISIOPATOLOGIA DA SOP
A SOP é uma síndrome heterogênea com a participação de múltiplos mecanismos fisiopatológicos, entretanto, o quanto cada um contribui para gerá-la ainda permanece desconhecido. A etiologia genética pode estar associada, uma vez que há uma maior frequência da síndrome em mães e irmãs de pacientes com SOP. Entretanto, o modelo de hereditariedade permanece incerto e desconhecido. Entre os mecanismos fisiopatológicos propostos, estão:
A resistência à insulina, ocasionando hiperinsulinemia. A insulina age diretamente nos receptores de insulina nos ovários, aumentando a produção de andrógenos por estímulo da 17-hidroxilase e aumento da produção de IGF-1, que também estimula a síntese de andrógenos e inibe a aromatase, diminuindo a conversão de andrógenos a estradiol. A insulina ainda diminui a produção hepática da globulina ligadora de hormônios sexuais (SHBG), aumentando a porção livre da testosterona;
B defeito primário neuroendócrino, ocasionando aumento da frequência de pulso e amplitude do LH, estimulando as células da teca a aumentarem a produção de andrógenos. Estes são convertidos em estrógenos nas células da granulosa ou nos tecidos periféricos. O estrogênio estimula a hipófise a manter liberação do LH e, promove feedback negativo na liberação de FSH. Com isso, ocorre uma maturação incompleta dos folículos;
C alteração no metabolismo do cortisol, diminuindo o retrocontrole central sobre a secreção de ACTH e, logo, seu aumento. Com isso resulta em maior estímulo adrenal à produção de andrógenos. Além disso, a insulina potencializa a produção de andrógenos pelas adrenais, mediada pelo ACTH.
O QUE É A SÍNDROME DOS OVÁRIOS POLICÍSTICOS?
A definição de SOP sempre foi controversa. A primeira padronização foi definida pela United States National Institutes of Health (NIH), em 1990, que incluía história clínica de anovulação crônica associada a evidências de hiperandrogenismo clínico e/ou laboratorial, na ausência de outras condições patogênicas como hiperplasia congênita da suprarrenal, doença de Cushing, hiperprolactinemia e tumores produtores de androgênios.
O segundo consenso, que até hoje é o mais aceito, foi definido em Rotterdam, em 2003, e estabelece que a SOP pode ser diagnosticada quando:
1. apresentar dois dos seguintes critérios:
A) oligomenorreia e/ou anovulação;
B) sinais clínicos e/ou bioquímicos de hiperandrogenismo;
C) ovários policísticos.
2. excluir outras causas de hiperandrogenismo, como tumores virilizantes, hiperplasia congênita da suprarrenal e a síndrome de Cushing.
Desde então esta é a definição mais aceita para a SOP. Em 2009, a Androgen Excess and PCOS Society criou uma nova definição, pela qual é necessária a presença dos três seguintes critérios:
1. hiperandrogenismo: hirsutismo e/ou hiperandrogenia;
2. oligo-anovulação e/ou ovários policísticos;
3. exclusão de outras causas de aumento de andrógenos ou doenças relacionadas: hiperplasia adrenal congênita, tumores secretores de andrógenos, uso de medicações androgênicas/anabólicas, síndrome de Cushing, disfunção tireoidiana e hiperprolactinemia.
Assim, podemos identificar quatro achados-chave no diagnóstico de SOP: sinais clínicos de hiperandrogenismo, hiperandrogenia, ovários policísticos e disfunção ovulatória/menstrual. Esses achados também têm definições padronizadas para se definir como um critério diagnóstico. Importante ressaltar também que SOP é sempre um diagnóstico de exclusão. As outras causas de hiperandrogenia e anovulação devem sempre ser descartadas para que se defina o diagnóstico.
Achados clínicos de hiperandrogenismo
Podem se manisfestar através de hirsutismo, acne e alopecia androgênica.
Hirsutismo: é a presença em mulheres de pelos terminais na face e/ou corpo com distribuição de padrão masculino. Essa queixa nem sempre é relatada pela paciente, mesmo quando está presente. Assim, deve-se avaliar pelo exame físico, por meio de uma pontuação visual. O método mais utilizado é uma modificação do método de Ferriman e Gallwey, pelo qual se avalia nove áreas: lábio superior, queixo, peito, costas, parte inferior das costas, abdômen superior e inferior, porção proximal do braço e coxa, atribuindo uma pontuação de 0-4 com base na densidade dos pelos. O valor de corte deve ser elaborado após o estudo de uma grande população de mulheres não selecionadas. Usando essa abordagem, em geral se considera hirsutismo um score ≥ 6, podendo variar para cada população, uma vez que a pilificação varia de acordo com a raça e etnia. O hirsutismo está presente em 65-75% das pacientes com SOP.
Acne: pode estar presente em 15-30% das pacientes com SOP, isoladamente ou acompanhada de hirsutismo.
Alopecia: é a queda em excesso de cabelos na região do couro cabeludo, levando à rarefação de pelos, causando grande repercussão estética e emocional para as pacientes. Sua prevalência é em torno de 10%.
Hiperandrogenia: é aumento dos níveis de andrógenos circulantes. O exame mais sensível é a dosagem da testosterona livre, que está aumentada em 70% das pacientes com SOP. Dosagem de testosterona total acrescenta pouco ao diagnóstico, mas quando > 150–200 ng/dL, é sugestivo de tumores produtores de andrógenos. Androstenediona está aumentada em somente cerca de 10% das pacientes. Sulfato de dehidroepiandrosterona (S-DHEA) apresenta aumento em 20-30% nestas mulheres, mas isoladamente em somente 10%. Dosagem de dehidroepiandrosterona (DHEA) apresenta pouco valor diagnóstico. 17(OH)progesterona também não costuma ter aumento, entretanto, deve sempre ser dosado, pois valores acima de 2,5 ng/mL na fase folicular indicam suspeita de hiperplasia adrenal congênita e exigem teste de ACTH para se excluir o diagnóstico.
Disfunção menstrual/ovulatória: cerca de 75% das pacientes apresentam sinais clínicos evidentes de anovulação, caracterizada por oligo/amenorreia. Entretanto, existe um grupo de 20-30% de pacientes com SOP que podem apresentar ciclos menstruais com poucas alterações, mesmo com anovulação. Diagnóstico de anovulação pode ser feito com ultrassom seriado e/ou dosagem de progesterona na fase lútea.
Ovários policísticos: os critérios de Rotterdam definem como ovários policísticos a presença de 12 ou mais folículos de 2-9 mm em cada um dos ovários por toda sua extensão e/ou volume ovariano aumentado (> 10 ml) de pelo menos um dos ovários. No entanto, em alguns estudos recentes, verificou-se que os limites normais de tamanho de ovário são < 7-7,5 cm3, e, por conseguinte, valores superiores a estes limites podem ser usados para indicar o aumento do tamanho do ovário. Pode ser visto ainda aumento do volume do estroma. Ovários com esse aspecto estão presentes em 75-90% das pacientes com SOP.
FIGURA 24-1. OVÁRIOS COM PADRÃO POLICÍSTICO
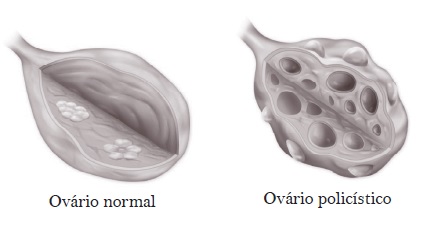
Outros achados clínicos que não entram nos critérios diagnósticos:
Elevação da relação LH/FSH: pacientes com SOP têm, com frequência, alterações na secreção de gonadotrofinas, com aumento da secreção de LH, resultante de uma frequência de pulso de GnRH/LH acelerado, enquanto os níveis de FSH são normais ou mesmo diminuídos. Muitas chegam até a ter uma relação LH:FSH >3:1.
Obesidade: pelo menos metade dessas mulheres estão acima do peso, isto é, o índice de massa corpórea (IMC) está acima dos 25 (lembrete: IMC = peso/altura ao quadrado). Este aumento de peso, em geral, é devido ao aumento da gordura visceral, ou seja, obesidade central, caracterizada por aumento da circunferência abdominal. Esse é um fator fundamental para futuras complicações desta doença. A circunferência abdominal superior a 88 cm está associada a um maior risco de problemas cardíacos (alguns já consideram o valor máximo de 80cm).
Resistência à insulina/hiperinsulinemia: está presente em 50-70% dos casos de SOP, principalmente se a paciente é obesa. A insulina aumentada leva ao aumento da produção de andrógenos pela teca, menor conversão de andrógenos a estradiol e diminuição na síntese de SHBG pelo fígado, aumentado a fração livre da testosterona. Os exames para investigar resistência à insulina são muito importantes para avaliar risco de possíveis complicações futuras, como diabetes mellitus, além de auxiliar na escolha do tratamento. Existem algumas dificuldades nesta avaliação, pois, até hoje, não existe um exame específico para o diagnóstico definitivo de resistência à insulina. Atualmente, a melhor opção é a dosagem da glicemia e a insulina em jejum, com posterior cálculo de HOMA-IR, que consiste em:
HOMA-IR: glicemia de jejum (em mmol/l) x insulina jejum (μU/ml) / 22,5 glicemia em mg/dl x 0,555= mmol/l
Os valores de referência do HOMA-IR variam de acordo com o IMC (Quadro 24-1).
QUADRO 24-1. VALORES DE REFERÊNCIA DO HOMA-IR DE ACORDO COM O IMC
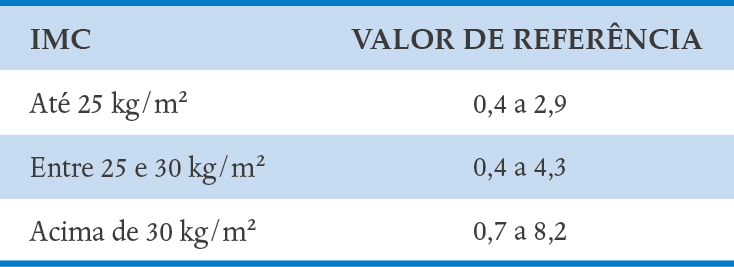
Infertilidade: como grande parte dessas pacientes apresenta anovulação, acaba apresentando infertilidade, sendo a principal causa de infertilidade por fator ovulatório (até 75%). Além disso, essas mulheres têm um maior índice de abortamento, provavelmente devido à resistência a insulina.
Acantosis nigricans: é aumento da pigmentação da pele (manchas escuras) em áreas de dobras, como pescoço, axilas e virilhas. Ocorre secundária à hiperinsulinemia e está presente em 1-3% das pacientes com SOP.
COMPLICAÇÕES A LONGO PRAZO
As principais complicações a longo prazo da SOP são:
Síndrome metabólica (ou plurimetabólica): chamada anteriormente de síndrome X, é uma doença da civilização moderna, relacionada à obesidade, que pode ocorrer em quase 50% das pacientes com SOP. Tem como base a resistência à ação de insulina, com a consequente hiperinsulinemia. É definida pela American Heart Association (AHA) e pelo National Heart, Lung, and Blood Institute (NHLBI) pela constatação de três ou mais das seguintes anormalidades:
QUADRO 24-2. CRITÉRIOS PARA SÍNDROME METABÓLICA EM MULHERES COM SOP (3 DE 5)
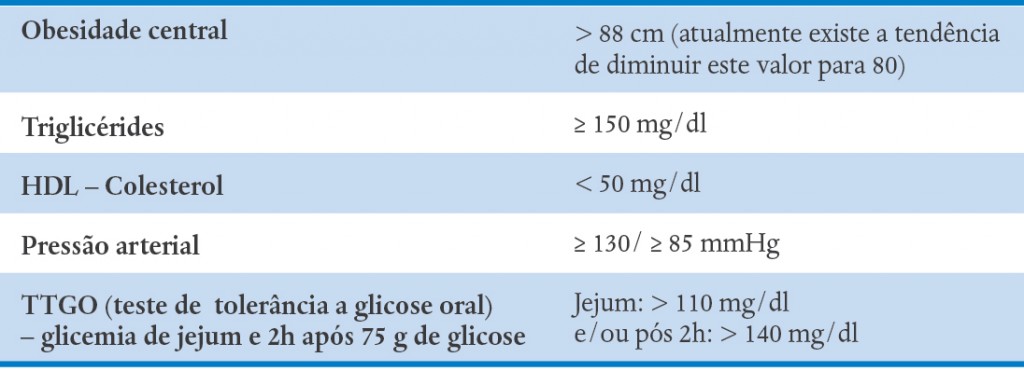
Seu diagnóstico é importante, uma vez que essas pacientes apresentam risco elevado de desenvolver doenças cardiovasculares (infarto e acidente vascular cerebral) e diabetes. A prevalência da síndrome metabólica em mulheres com SOP, na faixa etária dos 20 aos 40 anos, é de cerca de 40-50%. Em adolescentes, pelo menos 4 a 8% apresentam, mostrando que fatores de risco cardiovasculares podem ser verificados já nos primeiros anos da adolescência.
Diabetes: a resistência à insulina favorece o surgimento da diabetes. Este favorecimento pode ser ainda maior quando estiver acompanhado de obesidade. O controle de peso rigoroso e a dieta alimentar equilibrada diminuem a possibilidade desta complicação. Pelo menos 10% das mulheres com SOP desenvolvem diabetes tipo 2 por volta da quarta década da vida.
Doença cardiovascular: estima-se que mulheres com SOP apresentam risco 7,4 vezes mais alto de ocorrência de infarto do miocárdio. Isso é compreensível considerando a forte associação da SOP com diabetes, obesidade, hipertensão, hipertrigliceridemia, aumento de LDL e diminuição de HDL. Além disso, apresentam aumento do fator inibidor de ativação de fibrinogênio e aterosclerose. Todas essas modificações que ocorrem na SOP aumentam o risco de doença coronariana em idade precoce e acidente vascular cerebral. O que chama a atenção é que esse processo vascular degenerativo parece iniciar-se em faixas etárias bem precoces, uma vez que é possível detectar espessamento na camada íntima-média de carótidas das mulheres com SOP já entre os 18 e 22 anos de idade, mesmo naquelas com peso normal, sem dislipidemia ou hipertensão.
Câncer endometrial: o câncer endometrial é o quarto mais comum entre as mulheres e o mais frequente entre os do sistema reprodutivo feminino, quando não se consideram as mamas. A SOP pode aumentar a chance desta doença pelas alterações hormonais anovulatórias, com estímulo estrogênico prolongado sem a ação da progesterona.
Alterações do sono ou apneia noturna: alguns homens (17% a 24%) e algumas mulheres (5% a 9%) apresentam distúrbio do sono e repetidos episódios de dificuldade de respiração durante o mesmo. Este fato está frequentemente associado com obesidade, distribuição inadequada da gordura pelo corpo, resistência da insulina, hipertensão arterial e síndrome dos ovários policísticos, principalmente quando houver excesso de andrógenos.
EXAMES COMPLEMENTARES
1-Ultrassom: o ideal é ser realizado pela via transvaginal, mas, muitas vezes, é impossível de ser realizado, como em mulheres virgens. O diagnóstico de ovários policísticos por ultrassom não pode ser feito se a paciente estiver usando contraceptivos orais. Em mulheres com ciclos regulares, deve ser feito entre o terceiro e o quinto dia do ciclo.
2- Avaliação hormonal: para diagnóstico da síndrome e exclusão de outras causas de anovulação. Devem ser pedidos: • FSH e LH; • T4 livre e TSH; • prolactina;• cortisol;• androgênios: 17-Hidroxiprogesterona, testosterona total, testosterona livre, SHBG, SDHEA, androstenediona.
3- Avaliação metabólica
- perfil lipídico (colesterol total e frações e triglicérides);
- glicemia de jejum, insulina e cálculo de HOMA-IR;
- TTGO (se risco de síndrome metabólica).
TRATAMENTO
O tratamento da SOP baseia-se em regularizar o ciclo menstrual, reduzir hirsutismo/hiperandrogenismo, induzir ovulação em quem deseja a concepção, reduzir peso e fatores de risco para diabetes e doença cardiovascular.
1-Estilo de vida e terapia alimentar
A redução de peso deve ser recomendada a pacientes obesas ou com sobrepeso (IMC entre 25 e 30). Alguns estudos demonstram que a perda de 5-10% do peso corpóreo pode restaurar a ovulação e a fertilidade além de melhorar o colesterol, a pressão arterial, a resistência à insulina e diminuir as queixas de excesso de pelos e acne. Para isto é fundamental a modificação do estilo de vida, uma dieta balanceada e a prática de exercícios físicos de forma regular (principalmente aqueles que aumentem a circulação pélvica). Como nesta síndrome frequentemente existe o aumento da resistência à insulina, a melhor dieta é evitar alimentos ricos em carboidrato.
Dicas de alimentação
Evite ao máximo todas as formas de açúcar.
Evite ao máximo os carboidratos como o pão, as massas, o arroz, os cereais no café da manhã e os bolos, pois são rapidamente transformados em açúcares.
- Evite refrigerantes, sucos de frutas que possam elevar os níveis de açúcar, principalmente laranja, melancia e uva.
- Consuma quantidades adequadas de proteínas, mas tome cuidado com carnes que podem conter hormônios.
- Coma vegetal à vontade, frutas vermelhas, que não são muito doces (morango, framboesa, cereja, amora etc.) e alimentos integrais como arroz e aveia.
- Prefira leite e derivados desnatados ou light.
- Elimine álcool e cigarro.
- Aumente a quantidade de alimentos com fibra.
Terapia medicamentosa para perda de peso: para a perda de peso, pode ser útil ainda o uso de sensibilizantes da insulina como a metformina, com o benefício de combater a resistência à insulina. Em casos mais difíceis pode ser necessário o uso de medicamentos específicos, como Sibutramina, Orlistat e Rimonabant (um antagonista dos receptores endocanabinoides).
2- Tratamento da resistência à insulina
Além da perda de peso e mudanças de hábito, pacientes que apresentem resistência à insulina são beneficiadas com o uso de sensibilizadores da insulina, medicamentos que facilitam a passagem de glicose para o interior das células sem que haja necessidade de quantidade grande de insulina. A melhora dos padrões insulinêmicos colabora com a normalização dos padrões endócrino-reprodutivos, com a consequente regularização dos ciclos menstruais e ovulação. A droga mais utilizada para este fim é a metformina, uma biguanida que inibe a produção hepática de glicose e, consequentemente, melhora a hiperinsulinemia. A dose diária é de 1.500 a 2.000 mg. Quando utilizada sozinha, não aumenta a secreção de insulina e não causa hipoglicemia. Nas primeiras semanas pode produzir efeitos colaterais desagradáveis, como diarreia, náuseas, flatulência (gases), entretanto, uma nova formulação de liberação lenta (GLIFAGE-XR) pode ser tomada em dose única, três comprimidos no jantar, com efeitos mínimos indesejáveis. Os seus efeitos benéficos podem demorar meses para serem percebidos, mas a paciente não deve desanimar, pois este tempo de espera é normal. Estudos demonstram que o uso da metformina aumenta a frequência de ovulação espontânea, ciclos menstruais normais e resposta ovulatória ao tratamento com indutores de ovulação. A diminuição da resistência à insulina auxilia ainda, a longo prazo, na diminuição do hiperandrogenismo, com redução de até 25% na testosterona ativa em pacientes com SOP, em consequência da redução dos níveis plasmáticos de insulina.
Embora a metformina seja a droga mais utilizada para este fim, outros medicamentos com efeito semelhante têm sido adotados. Entre eles estão: tiazolinedionas (Troglitazona, Pioglitazona, Rosiglitazona), D-chiro-inositol e myo-inositol.
As tiazolinedionas (troglitazona, roziglitazona e pioglitazona) são outro grupo de sensibilizadores da insulina. A primeira aprovada foi a troglitazona, subsequentemente retirada do mercado devido a efeitos hepatotóxicos. Em estudos, a administração de rosiglitazona 4 mg/dia ou de pioglitazona 30 mg/dia a mulheres obesas e não obesas com SOP levaram a uma melhora da resistência à insulina, diminuição da produção androgênica ovariana e restauração da ovulação espontânea. As tiazolinedionas estão associadas a um pequeno ganho ponderal (1 a 2 kg), redução moderada do hematócrito, ligeiro aumento do volume plasmático e edema. Tanto a rosiglitazona como a pioglitazona são classificadas como fármacos de categoria C, portanto, as mulheres tratadas com esses medicamentos devem receber aconselhamento contraceptivo e interromper o tratamento na ocorrência de gestação.
D-chiro-inositol e myo-inositol são isômeros do inositol, substância mediadora de vários processos celulares. Pacientes com SOP podem apresentar deficiência da enzima que produz o inositol no organismo. Sua função é melhorar a ação da insulina, reduzindo, assim, a resistência a esta, o hiperandrogenismo e normalizando os ciclos menstruais.
3- Regularização do ciclo menstrual
A escolha do tipo de medicamento vai depender do objetivo da paciente. Se ela não quiser ter filhos e apresentar irregularidade menstrual, os anticoncepcionais poderão ser uma boa escolha. Eles regularizam o ciclo, protegem o endométrio do estímulo estrogênico sem antagonismo da progesterona e diminuem o hiperandrogenismo. Isso ocorre pois: diminuem o LH e a consequente produção de andrógenos ovarianos; o componente estrogênico aumenta a produção de SHBG e, assim, diminui a fração livre e ativa dos andróginos; e o componente progestagênico inibe a atividade da 5α-redutase (que converte testosterona na forma mais ativa, dihidrotestosterona).
Na escolha do anticoncepcional, deve-se usar aqueles com progestágenos não androgênicos (como noretindrona, desogestrel e norgestimate) ou aqueles com ação antiandrogênicas, como drospirenona, dienogeste e principalmente ciproterona (Diane, Selene e Diclin).
4- Combate do hiperandrogenismo
O tratamento do hiperandrogenismo pode ser feito com medicamentos que diminuem a produção de andrógenos (como os anticoncepcionais) ou que bloqueiam sua ação (substâncias antiandrogênicas). Os antiandrogênios são medicações que se ligam aos receptores androgênicos intracelulares ou inibem enzimas importantes para o metabolismo dos andrógenos nos órgãos-alvo, como a 5α-redutase. São indicados o acetato de ciproterona, a espironolactona, a flutamida, a finasterida e a eflornitina (creme de aplicação local que reduz a quantidade de pelos).
Devem ser utilizados preferencialmente em associação com algum método contraconceptivo, pois podem interferir no desenvolvimento fetal, caso uma gestação ocorra durante seu uso.
O acetato de ciproterona na dose de 2 mg/dia é a opção mais usada, principalmente por ter formulações em associação ao etinil-estradiol (Diane, Selene e Diclin). Tem como mecanismo de ação a inibição do receptor intracelular dos andrógenos. Seu efeito cutâneo é importante, levando à melhora razoável do hirsutismoe e da acne após três meses de tratamento, assim como da alopecia. Efeitos colaterais podem ser: fadiga, diminuição da libido e, às vezes, ganho de peso.
A espironolactona é um antiandrogênico que pode ser usado em dosagens entre 25 e 200 mg/dia. Interfere na produção adrenal e ovariana de androgênios, liga-se aos receptores intracelulares dos andrógenos e inibe a enzima 5α-redutase. Pode ocasionar alterações eletrolíticas (principalmente se associada a drospirenona, que tem ação antimineralocorticoide) e sangramento uterino disfuncional, se não associada a um anticoncepcional. A finasterida inibe a enzima 5α-redutase, diminuindo a conversão de testosterona em dihidrotestosterona. A dose recomendada é 2,5-5 mg/dia.
A flutamida tem ação parecida com a espironolactona e pode ser utilizada em doses entre 250-500 mg/dia. Por seu efeito hepatotóxico deve ser utilizada somente quando outras terapias não obtiveram o sucesso esperado. Em casos de hirsutismo e acne muito intensos, pode ser necessário acompanhamento paralelo com dermatologista, para uso de laser e medicamentos específicos.
5- Tratamento da infertilidade
No tratamento da infertilidade, como nos casos anteriores, a primeira linha de tratamento é a perda de peso, que às vezes isoladamente já faz a paciente apresentar ciclos ovulatórios. Além disso, a obesidade está associada a maior risco de aborto e diminuição do sucesso nos tratamentos. Se houver resistência à insulina, metformina também ajuda na recuperação de ciclos ovulatórios, melhor resposta aos indutores de ovulação e diminuição do risco de aborto.
Para indução da ovulação, citrato de clomifeno é a primeira escolha pelo baixo custo, facilidade de usar e taxa de ovulação de 70-80% por ciclo, com gravidez cumulativa após seis meses de até 50-60% quando única causa de infertilidade. Opções ao clomifeno é o uso de inibidores da aromatase e gonadotrofinas injetáveis em diferentes esquemas de indução, dando prioridade para aquelas compostas somente de FSH, sem componente LH.
Outra opção, quando o ovário é resistente aos esquemas de indução de ovulação, é o tratamento cirúrgico chamado drilling ovariano. Sob laparoscopia, realiza-se de quatro a dez furos na superfície e estroma dos ovários com eletrocautério. Cerca de 90% das pacientes normalizam ciclos após o procedimento. Há o inconveniente de ser um procedimento cirúrgico e a preocupação de causar aderências pélvicas, levando a um fator a mais de infertilidade.
Quando optado por FIV, pacientes com SOP apresentam taxas de sucesso semelhante às que não apresentam a síndrome, entretanto um risco aumentado para SHO. Por isso, muito cuidado deve ser tomado na indução ovariana dessas pacientes, dando prioridade para ciclo com antagonista, com baixa dose inicial de gonadotrofina (de preferência FSH recombinante) e trigger final com análogo de GnRH.
Uma opção para melhora da fertilidade de pacientes com SOP é o uso de myo-inositol. Além da melhora metabólica já descrita, por ampliar a resistência à insulina, nos tratamentos de FIV também tem benefícios: reduz a quantidade de FSH necessária para estimulação ovariana, diminui o número de dias de estimulação, abaixa a chance de hiperestimulação ovariana, melhora a qualidade dos óvulos e melhora a qualidade dos embriões.
CONCLUSÃO
A SOP é uma síndrome complexa que tem várias possíveis origens e uma delas é a resistência à insulina. Por isso o foco do tratamento deve ser o combate a esta alteração. A SOP não pode ser prevenida, mas quanto mais precoce for o diagnóstico, menor será a chance de complicações futuras.
Já na adolescência podem ser notados os sinais desta síndrome e, por isso, além dos fatores hereditários que podem prenunciar o surgimento futuro desta doença (mãe e irmãs), deve-se estar atento à obesidade, à quantidade de pelos no corpo e ao padrão menstrual alterado, geralmente longo, alterações estas que podem ser notadas pelos pais ou pelo ginecologista geral.
A síndrome dos ovários policísticos deve ser diagnosticada e tratada já na adolescência devido às complicações reprodutivas, metabólicas e oncológicas que podem estar associadas a ela. O melhor tratamento preventivo é uma dieta alimentar equilibrada e um estilo de vida saudável.
